El estudio, publicado este miércoles en la revista 'Nature', abre la puerta para el desarrollo de una nueva clase de objetivos farmacológicos para el cáncer, así como enfermedades inflamatorias, como es el caso de la artritis reumatoide, la enfermedad de Crohn y la psoriasis.
"Nuestra nueva investigación revela que la estructura totalmente activa de una ligasa E3 RBR tiene un potencial terapéutico importante en oncología e inmunología -resume Bernhard Lechtenberg. investigador postdoctoral en el SBP y autor principal del estudio-.La estructura tridimensional que presentamos proporciona información detallada de la arquitectura molecular del complejo y nos permite sacar conclusiones sobre cómo funciona".
La ubiquitina es una pequeña proteína que ayuda a regular la función de otras proteínas en el cuerpo. Las ligasas E3 realizan un proceso conocido como ubiquitinación, donde la ubiquitina se une a una proteína sustrato, cambiando la forma en que funciona. Hay tres clases de ligasas E3, pero los miembros del tipo RBR han surgido recientemente como una nueva y relativamente sin explotar clase de objetivos para el descubrimiento de fármacos, debido a su papel en la modulación del sistema inmune.
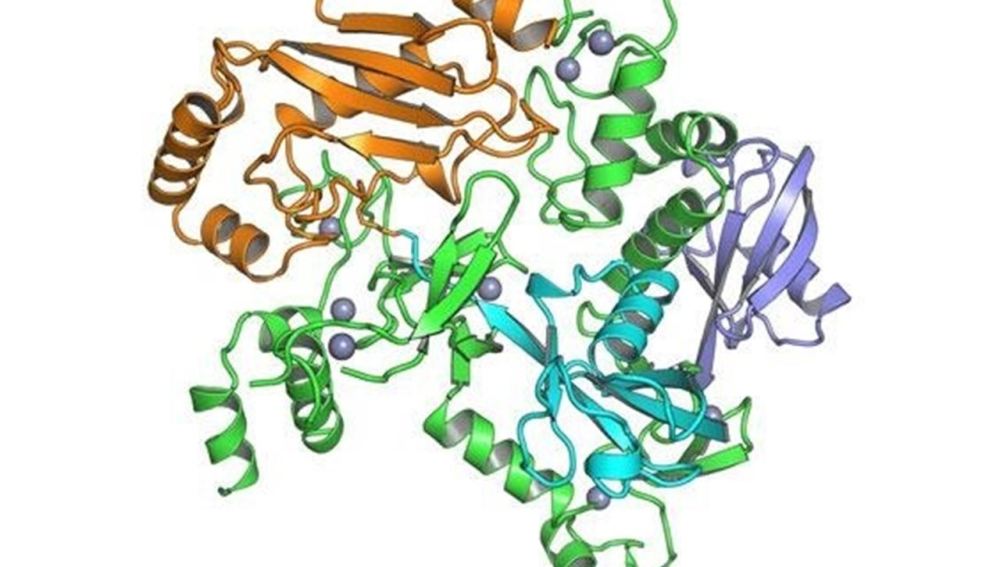
"Nos sorprendimos al encontrar cómo la forma activa de la ligasa E3 que analizamos, llamada HOIP, se una a la ubiquitina de una manera muy diferente -de forma alargada- en comparación con los otros tipos de ligasas E3 -apunta Stefan Riedl, de SBP y autor principal del artículo-. Esto puede ser clave para su papel en la activación de la vía NF-kB, un proceso de señalización que está bien establecido como un regulador de la supervivencia celular y la muerte, y ayuda a coordinar el sistema inmunológico.
"NF-kB es el regulador maestro de la inflamación dentro de las células y se cree que su activación promueve el desarrollo del cáncer mediante la inhibición de la muerte celular y la promoción de la inflamación. Este estudio elimina una barrera técnica significativo que ha impedido explotar las ligasas RBR E3 como una diana farmacológica para el cáncer y trastornos inflamatorios. Nuestro próximo paso es seguir trabajando muy de cerca con nuestros colaboradores de biología e inmunología para entender más a fondo la regulación de las ligasas E3 RBR", añade Riedl.
UN ESTUDIO PUBLICADO EN LA REVISTA 'NATURE'
UN ESTUDIO PUBLICADO EN LA REVISTA 'NATURE'
Investigan nuevas terapias contra el cáncer y las enfermedades inflamatorias
Un grupo de científicos del instituto de investigación Médica Sandford-Burnham Prebys (SBP), en Estados Unidos, han resuelto la estructura atómica de un complejo único de ligasa ubiquitina. La ubiquitina es conocida por su papel en la degradación de proteínas, pero recientemente se ha descubierto su importancia para la señalización celular, la reparación del ADN, la respuesta inmune y las propiedades anti-inflamatoria.
Los mas vistos
-
1
Compromiso Atresmedia
Una nueva estrategia de vacuna basada en ARN es eficaz para todas las cepas de un virus
-
2
Compromiso Atresmedia
Los diez avances científicos más destacados de 2023
-
3
Compromiso Atresmedia
Los fondos recaudados por el reto 'Ice Bucket Challenge' han servido para descubrir el gen que provoca ELA
