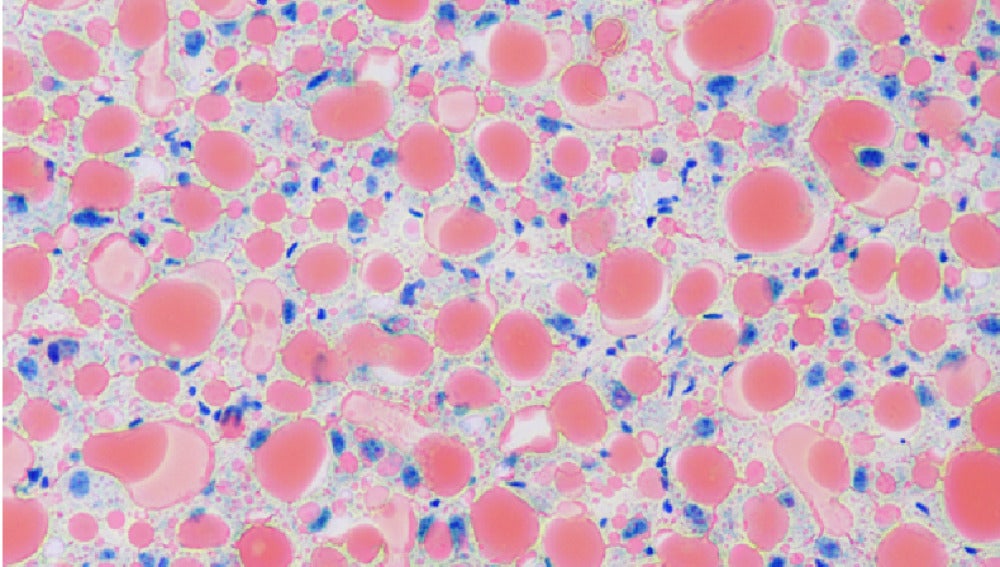
El hígado de estos pacientes produce más glucosa, grasas y proteínas desfavorables, como la hepatokine fetuin-A, que se libera en el torrente sanguíneo. De esta manera, las sustancias secretadas del hígado graso entran en otros órganos y provocan reacciones.
Hasta ahora no se sabía qué efectos tenía esta diafonía de órganos, qué órganos eran los más afectados y cuál era el daño causado por la hepatokine fetuín-A.
Los científicos analizaron la influencia de fetuin-A en el tejido adiposo pancreático. Observaron que, aproximadamente, un tercio del tejido adiposo pancreático se compone de células precursoras adiposas, un tipo de células madre, además de las células adiposas maduras.
Si estas células son tratadas con fetuina-A en cultivos celulares, las precursoras produce marcadores de inflamación y factores de atracción de células inmunes.
Se analizaron muestras de tejido de 90 pacientes, y encontraron que la proporción de la grasa pancreática variaba en gran medida. El número de células de defensa del sistema inmunológico se incrementó significativamente en áreas donde se habían acumulado muchas células adiposas.
Asimismo, en 200 sujetos con un mayor riesgo de diabetes tipo 2, el contenido de grasa pancreática se midió mediante resonancia magnética, comparando los resultados con los parámetros de la diabetes. Así, encontraron que en personas que ya habían experimentado un empeoramiento en la regulación de la glucosa en sangre, el aumento de la degeneración grasa pancreática ocasionaba una secreción de insulina reducida.
Los científicos han extraído como resultado que, en lugar de proteger el tejido como antes, el tejido adiposo ahora provoca procesos inflamatorios, lo que conduce a una restricción de la función renal.